Chaque année, la grippe touche entre 2 et 6 millions de personnes en France et entraîne environ 10 000 décès, principalement parmi les populations les plus fragiles, selon l’Institut Pasteur. Si la vaccination reste le principal outil de prévention, la recherche explore d’autres approches pour lutter contre le virus, notamment en ciblant son génome afin de perturber son cycle de réplication.
Dans cette optique, une équipe de biologistes français est parvenue, pour la première fois, à observer et modéliser la structure de son génome. Ces travaux, publiés le 14 décembre 2024 dans la revue Nucleic Acids Research, apportent un nouvel éclairage sur l’organisation du génome du virus et ouvrent la voie au développement de nouvelles stratégies antivirales. Entretien avec Thibaut Crépin, directeur de recherche au CNRS associé à l’Université Grenoble-Alpes, qui a dirigé cette étude.
Vous êtes directeur de recherche au CNRS et spécialiste du virus de la grippe. Quel a été votre parcours et quels sont vos axes de recherche ?
J’ai rejoint l’institution en 2007, suivant un parcours classique : d’abord en tant que chargé de recherche, puis en tant que directeur de recherche. Mon domaine de spécialisation est la biologie structurale, et mes travaux portent principalement sur le virus de la grippe. Mon objectif est de comprendre le fonctionnement des virus qu’étudient mon équipe dans la cellule, et plus particulièrement leur mécanisme de réplication.
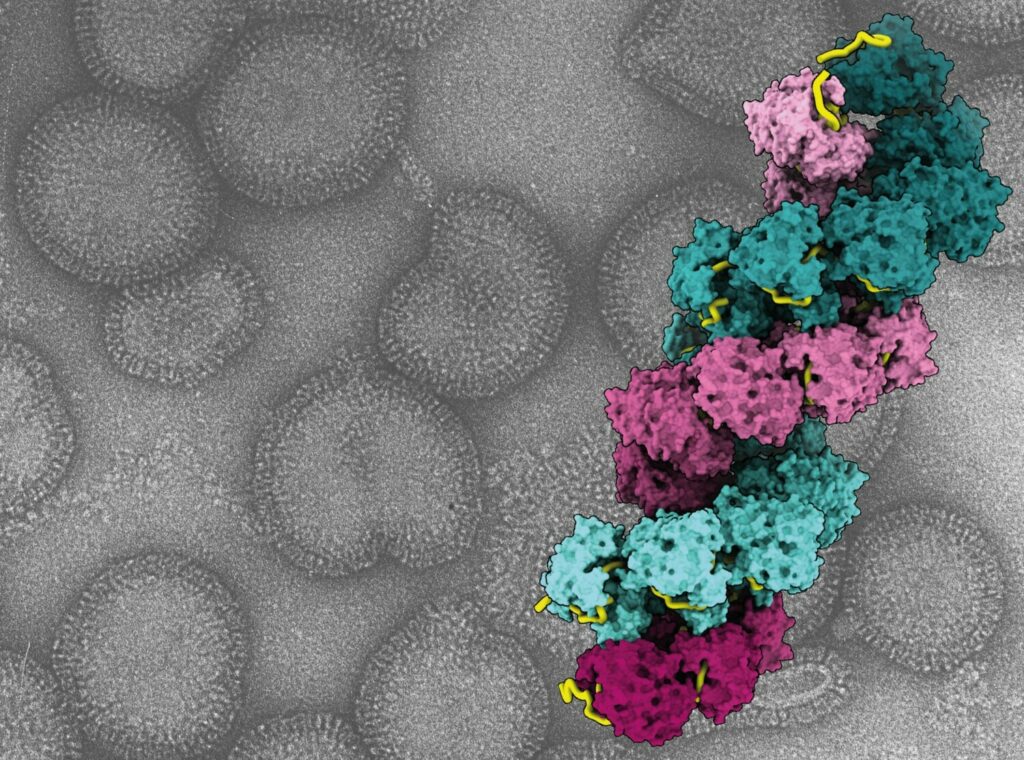
Nous nous intéressons au génome du virus de la grippe, qui est un génome ARN. Celui-ci a une particularité : lorsqu’il est nu, il ne peut être infectieux. Il doit donc impérativement se trouver sous une forme spécifique appelée ribonucléoprotéine (RNP). Cette RNP est composée de l’ARN viral recouvert par une protéine, la nucléoprotéine, tandis que ses deux extrémités sont associées à l’ARN polymérase virale. C’est cette structure ARN-nucléoprotéine, associée à l’ARN polymérase, qui permet la réplication du virus dans la cellule.
Depuis mon entrée au CNRS, je travaille sur cette thématique. Nous avons d’abord étudié la polymérase seule, puis la nucléoprotéine seule. Ces dernières années, nous cherchons à comprendre comment la nucléoprotéine se fixe sur l’ARN pour le protéger. Elle joue un rôle clé en protégeant l’ARN viral contre le système immunitaire, qui pourrait sinon le dégrader. C’est pour cette raison que l’ARN viral est en permanence recouvert de nucléoprotéines.
Jusqu’à nos travaux récents, personne n’avait réussi à observer directement le complexe formé entre la nucléoprotéine et l’ARN, et donc à comprendre précisément comment cette protection du génome viral s’opère.
Votre équipe travaille sur la nucléoprotéine depuis de nombreuses années. Quelles ont été les étapes clés qui ont permis d’aboutir à l’observation de son interaction avec l’ARN ?
Ce travail s’est déroulé en plusieurs étapes. La personne avec qui je travaille étudie la nucléoprotéine depuis quarante ans. Pour ma part, je suis arrivé en 2007 et j’ai toujours entendu parler de la nécessité de visualiser l’interaction entre l’ARN et la nucléoprotéine.
Entre 2010 et 2014, nous avons étudié la nucléoprotéine seule pour mieux comprendre son fonctionnement.
Ensuite, entre 2015 et 2018, nous avons analysé son interaction avec l’ARN. En ajustant certains paramètres, nous avons réussi à observer comment la nucléoprotéine s’organise autour de l’ARN et adopte une structure semblable à celle que l’on trouve dans le virus. Ces recherches ont été finalisées grâce aux travaux de thèse de Florian Chenavier, qui a permis d’obtenir la structure de cette nucléoprotéine au sein de la ribonucléoprotéine virale.
Quelles perspectives ouvre cette découverte ?
Nous avons confirmé que le génome de la grippe comprend huit molécules d’ARN sous forme de RNP, toutes indispensables au fonctionnement du virus. Si l’une d’elles manque, le virus devient non fonctionnel. Pendant longtemps, nous avons spéculé sur la manière dont ces RNP interagissent entre elles. Nos travaux récents nous apportent un nouvel éclairage sur ce mécanisme, ce qui est crucial pour comprendre la formation des particules virales.
D’un point de vue appliqué, cela signifie que nous pouvons maintenant chercher des molécules capables d’interférer avec l’interaction ARN-nucléoprotéine. Nous collaborons avec des chimistes pour identifier des composés qui viendraient se fixer à la place de l’ARN et ainsi perturber la formation des RNP. Si nous parvenons à déstabiliser ces structures, nous pourrions empêcher la réplication du virus.
L’objectif est de développer de nouveaux antiviraux qui viendraient cibler la nucléoprotéine, en particulier les régions qui interagissent avec l’ARN viral. En perturbant cette interaction, nous pourrions empêcher la réplication du virus et ainsi limiter l’infection.
Le virus de la grippe est connu pour évoluer constamment. En quoi cette variabilité constitue-t-elle un défi pour la prévention et la lutte contre l’infection ?
Ce qui rend le virus dangereux, c’est justement sa capacité à muter. Ce phénomène ne concerne pas seulement la grippe, mais l’ensemble des virus à ARN, qui évoluent très rapidement.
Lorsqu’un virus mute, le système immunitaire de l’hôte n’est plus parfaitement adapté à la nouvelle souche. C’est d’ailleurs l’une des raisons pour lesquelles les vaccins n’ont pas une efficacité durable contre une seule et même souche virale.
Dans le cas de la grippe, cela explique pourquoi une vaccination annuelle est nécessaire. Le virus évolue constamment, et à chaque mutation, l’efficacité du système immunitaire diminue face à la nouvelle version du virus.
Quelles sont les prochaines étapes de vos recherches ?
Notre priorité est d’identifier des molécules capables d’interférer avec l’interaction ARN-nucléoprotéine. Nous avons déjà commencé à tester certaines pistes grâce à notre collaboration avec des chimistes. L’enjeu est maintenant de vérifier leur efficacité et d’approfondir notre compréhension de la dynamique des RNP. Ces avancées pourraient ouvrir la voie à de nouveaux traitements antiviraux ciblant directement les mécanismes fondamentaux de la grippe.













Modération par la rédaction de VousNousIls. Conformément à la loi relative à l'informatique, aux fichiers et aux libertés, vous disposez d'un droit d'accès, de modification, de rectification et de suppression des données vous concernant. Pour exercer ce droit adressez-vous à CASDEN Banque Populaire – VousNousIls.fr 1 bis rue Jean Wiener – Champs-sur-Marne 77447 Marne-la-Vallée Cedex 2.